Những câu hỏi liên quan
Hỗn hợp rắn X gồm M, MO và MCl2 (M là kim loại có hóa trị II không đổi). Cho 18,7 gam X tác dụng với dung dịch HCl (vừa đủ), thu được dung dịch A và 6,72 lít khí (đktc). Cho dung dịch NaOH dư vào dung dịch A, sau phản ứng thu được kết tủa B. Nung B ở nhiệt độ cao đến khối lượng không đổi thu được 18,0 gam chất rắn. Mặt khác, khi cho 18,7 gam hỗn hợp X vào 500 ml dung dịch CuCl2 1,0M, sau phản ứng, tách bỏ chất rắn rồi cô cạn dung dịch, thu được 65,0 gam muối khan. Biết các phản ứng hóa học xảy r...
Đọc tiếp
Hỗn hợp rắn X gồm M, MO và MCl2 (M là kim loại có hóa trị II không đổi). Cho 18,7 gam X tác dụng với dung dịch HCl (vừa đủ), thu được dung dịch A và 6,72 lít khí (đktc). Cho dung dịch NaOH dư vào dung dịch A, sau phản ứng thu được kết tủa B. Nung B ở nhiệt độ cao đến khối lượng không đổi thu được 18,0 gam chất rắn. Mặt khác, khi cho 18,7 gam hỗn hợp X vào 500 ml dung dịch CuCl2 1,0M, sau phản ứng, tách bỏ chất rắn rồi cô cạn dung dịch, thu được 65,0 gam muối khan. Biết các phản ứng hóa học xảy ra hoàn toàn.
Xác định kim loại M và tính thành phần phần trăm theo khối lượng của các chất có trong hỗn hợp X.
Cho 8 gam hỗn hợp A gồm Mg và kim loại R tác dụng với dung dịch HCl dư thu được 4,48 lít khí (đktc). Nếu cho 9,6 gam hỗn hợp A phản ứng với khí clo dư thì thu được 30,9 gam hỗn hợp muối. a. Xác định tên kim loại R. Biết các phản ứng hóa học đều xảy ra hoàn toàn.
Đặt a,b là số mol Mg, R trong 8 gam A. Đặt x,y là hoá trị thấp cao của R
mA = 24a + bR = 8 (1)
Với HCl -> 2a + bx = 0,2 .2 (2)
Trong 9,6 gam A ( gấp 1,2 lần 8 gam A ) chứa 1,2a và 1,2b mol Mg, R
Với Cl2 -> 2 . 1,2a + 1,2by = 2 ( 30,9 - 9,6 ) / 71 (3)
Với 1 ≤ x ≤ y ≤ 3 -> Chọn x = 2; y = 3
(2)(3) -> a = b = 0,1
(1) -> R= 56 -> = Fe
Đúng 1
Bình luận (0)
Đốt 3,72 gam hỗn hợp X gồm 2 kim loại Al và Mg trong bình đựng khí Clo, sau một thờigian phản ứng thu được 10,82 gam hỗn hợp Y gồm 4 chất rắn. Cho hỗn hợp Y tác dụng với dungdịch H2SO4 loãng dư, sau phản ứng hoàn toàn thu được khí H2. Dẫn toàn bộ lượng H2 sinh ra đi quaống đựng 8 gam CuO nung nóng, sau một thời gian thấy trong ống còn lại 6,72 gam chất rắn ( chỉ có80% H2 tham gia phản ứng). Xác định % khối lượng mỗi kim loại trong hỗn hợp X.
Đọc tiếp
Đốt 3,72 gam hỗn hợp X gồm 2 kim loại Al và Mg trong bình đựng khí Clo, sau một thời
gian phản ứng thu được 10,82 gam hỗn hợp Y gồm 4 chất rắn. Cho hỗn hợp Y tác dụng với dung
dịch H2SO4 loãng dư, sau phản ứng hoàn toàn thu được khí H2. Dẫn toàn bộ lượng H2 sinh ra đi qua
ống đựng 8 gam CuO nung nóng, sau một thời gian thấy trong ống còn lại 6,72 gam chất rắn ( chỉ có
80% H2 tham gia phản ứng). Xác định % khối lượng mỗi kim loại trong hỗn hợp X.
Để tác dụng vừa đủ với m gam hỗn hợp X gồm Cr và kim loại M có hóa trị không đổi cần vừa đúng 2,24 lít hỗn hợp khí Y (đktc) gồm O2 và Cl2 có tỷ khối đối với H2 là 27,7 thu được 11,91 gam hỗn hợp Z gồm các oxit và muối clorua. Mặt khác, cho m gam hỗn hợp X tác dụng với một lượng dư dung dịch HNO3 đặc, nguội thu được 2,24 lít khí NO2 (đktc) là sản phẩm khử duy nhất. Các phản ứng xảy ra hoàn toàn. Kim loại M là: A. Ca B. Cu C. Mg D. Zn
Đọc tiếp
Để tác dụng vừa đủ với m gam hỗn hợp X gồm Cr và kim loại M có hóa trị không đổi cần vừa đúng 2,24 lít hỗn hợp khí Y (đktc) gồm O2 và Cl2 có tỷ khối đối với H2 là 27,7 thu được 11,91 gam hỗn hợp Z gồm các oxit và muối clorua. Mặt khác, cho m gam hỗn hợp X tác dụng với một lượng dư dung dịch HNO3 đặc, nguội thu được 2,24 lít khí NO2 (đktc) là sản phẩm khử duy nhất. Các phản ứng xảy ra hoàn toàn. Kim loại M là:
A. Ca
B. Cu
C. Mg
D. Zn
Đáp án D
Có

m g X + HNO3 đặc nguội → 0,1 mol NO2
→ BTe a . n M = 0 , 1 m o l ( 2 )
Từ (1) và (2) suy ra:
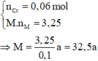
=> a = 2, M = 65 (M là Zn).
Đúng 0
Bình luận (0)
Cho hỗn hợp bột các kim loại FA là kim loại có hóa trị n hòa tan bằng dung dịch HCl vừa đủ thì thu được 7,84 lít khí ở điều kiện tiêu chuẩn hỗn hợp trên tác dụng với 8,4 lít khí Clo điều kiện tiêu chuẩn thì phản ứng xảy ra hoàn toàn biết rằng hỗn hợp đêm trộn 1:4a) xác định hóa trị và thanh kim loại a biết khối lượng a bằng 5,4 gamb) tính thể tích khí clo để hòa hợp với kim loại a và khối lượng dung dịch HCl 36% Cần cho phản ứng trên
Đọc tiếp
Cho hỗn hợp bột các kim loại FA là kim loại có hóa trị n hòa tan bằng dung dịch HCl vừa đủ thì thu được 7,84 lít khí ở điều kiện tiêu chuẩn hỗn hợp trên tác dụng với 8,4 lít khí Clo điều kiện tiêu chuẩn thì phản ứng xảy ra hoàn toàn biết rằng hỗn hợp đêm trộn 1:4
a) xác định hóa trị và thanh kim loại a biết khối lượng a bằng 5,4 gam
b) tính thể tích khí clo để hòa hợp với kim loại a và khối lượng dung dịch HCl 36% Cần cho phản ứng trên
1. Cho x gam một muối halogenua của một kim loại kiềm tác dụng với 200ml dd H2SO4 đặc, nóng vừa đủ. Sau khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp sản phẩm A trong đó có một khí B (mùi trứng thối). Cho khí B tác dụng với dd Pb(NO3)2 (dư) thu được 47,8 gam kết tủa màu đen. Phần sản phẩm còn lại, làm khô thu được 342,4 gam chất rắn T. Nung T đến khối lượng không đổi thu được 139,2 gam muối duy nhất.a. Tính nồng độ mol/lit của dd H2SO4 ban đầu.b. Xác định công thức phân tử của muối halogenua v...
Đọc tiếp
1. Cho x gam một muối halogenua của một kim loại kiềm tác dụng với 200ml dd H2SO4 đặc, nóng vừa đủ. Sau khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp sản phẩm A trong đó có một khí B (mùi trứng thối). Cho khí B tác dụng với dd Pb(NO3)2 (dư) thu được 47,8 gam kết tủa màu đen. Phần sản phẩm còn lại, làm khô thu được 342,4 gam chất rắn T. Nung T đến khối lượng không đổi thu được 139,2 gam muối duy nhất.
a. Tính nồng độ mol/lit của dd H2SO4 ban đầu.
b. Xác định công thức phân tử của muối halogenua và tính x.
2. Cho M là kim loại tạo ra hai muối MClx, MCly và tạo ra 2 oxit MO0,5x, M2Oy có thành phần về khối lượng của Clo trong 2 muối có tỉ lệ 1 : 1,173 và của oxi trong 2 oxit có tỉ lệ 1 : 1,352.
a. Xác định tên kim loại M và công thức hóa học các muối, các oxit của kim loại M.
b. Viết các phương trình phản ứng khi cho M tác dụng lần lượt với MCly; H2SO4 đặc, nóng.
1)
a) Khí B mùi trứng thối => H2S
$Pb(NO_3)_2 + H_2S \to PbS + 2HNO_3$
n H2S = n PbS = 47,8/239 = 0,2(mol)
Gọi CTHH của muối halogen là RX
8RX + 5H2SO4 đặc,nóng → 4R2SO4 + H2S + 4X2 + 4H2O
n H2SO4 = 5n H2S = 0,2.5 = 1(mol)
CM H2SO4 = 1/0,2 = 5M
T gồm R2SO4,X2
Khi nung thì chỉ còn lại R2SO4
=> m X2 = 342,4 - 139,2 = 203,2(gam)
n X2 = 4n H2S = 0,8(mol)
=> M X2 = 2X = 203,2/0,8 = 254
=> X = 127(Iot)
Theo PTHH :
n R2SO4 = n X2 = 0,8(mol)
=> M R2SO4 = 2R + 96 = 139,2/0,8 = 174
=> R = 39(Kali)
Vậy Muối cần tìm là $KI$
n KI = 2n R2SO4 = 1,6(mol)
=> x = 1,6.166 = 265,6 gam
Đúng 3
Bình luận (0)
Cho 3,64 gam hỗn hợp E gồm một oxit, một hiđroxit và một muối cacbonat trung hòa của một kim loại M có hóa trị II tác dụng vừa đủ với 117,6 gam dung dịch H2SO4 10%. Sau phản ứng, thu được 0,448 lít khí (đktc) và dung dịch muối duy nhất có nồng độ 10,867% (khối lượng riêng là 1,093 gam/ml); nồng độ mol là 0,545M. a) Viết các phương trình phản ứng xảy ra và xác định kim loại M. b) Tính % khối lượng của các chất có trong hỗn hợp E.
Đọc tiếp
Cho 3,64 gam hỗn hợp E gồm một oxit, một hiđroxit và một muối cacbonat trung hòa của một kim loại M có hóa trị II tác dụng vừa đủ với 117,6 gam dung dịch H2SO4 10%. Sau phản ứng, thu được 0,448 lít khí (đktc) và dung dịch muối duy nhất có nồng độ 10,867% (khối lượng riêng là 1,093 gam/ml); nồng độ mol là 0,545M.
a) Viết các phương trình phản ứng xảy ra và xác định kim loại M.
b) Tính % khối lượng của các chất có trong hỗn hợp E.
a) Đặt số mol của MO, M(OH)2, MCO3 tương ứng là x, y, z.
Nếu tạo muối trung hòa ta có các phản ứng:
MO + H2SO4 →MSO4 + H2O (1)
M(OH)2 + H2SO4 →MSO4 + 2H2O (2)
MCO3 + H2SO4 →MSO4 + H2O + CO2 (3)
Nếu tạo muối axít ta có các phản ứng:
MO + 2H2SO4 →M(HSO4)2 + H2O (4)
M(OH)2 + 2H2SO4 →M(HSO4)2 + 2H2O (5)
MCO3 + 2H2SO4 →M(HSO4)2 + H2O + CO2 (6)
Ta có :
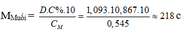
– TH1: Nếu muối là MSO4 M + 96 = 218 M = 122 (loại)
– TH2: Nếu là muối M(HSO4)2 M + 97.2 = 218 M = 24 (Mg)
Vậy xảy ra phản ứng (4, 5, 6) tạo muối Mg(HSO4)2
b) Theo (4, 5, 6) Số mol CO2 = 0,448/22,4 = 0,02 molz = 0,02 (I)
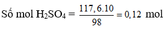
2x + 2y + 2z = 0,12 (II)
Đề bài: 40x + 58y + 84z = 3,64 (III)
Giải hệ (I, II, III): x = 0,02; y = 0,02; z = 0,02
%MgO = 40.0,02.100/3,64 = 21,98%
%Mg(OH)2 = 58.0,02.100/3,64 = 31,87%
%MgCO3 = 84.0,02.100/3,64 = 46,15%
Đúng 0
Bình luận (0)
Cho 17,3 gam hỗn hợp gồm 2 kim loại Al và Zn tác dụng với 400 gam dung dịch HCl. Sau khi phản ứng xảy ra hoàn toàn (các chất phản ứng vừa đủ) thì thu được 15,68l H2 (đktc) a. viết phương trình phản ứng xảy ra b.Tính % khối lượng mỗi kim loại trong hỗn hợp ban đầu c. Tính C% mỗi muối thu được sau phản ứng
Cho 2,24 lít (đktc) hỗn hợp gồm
C
l
2
v
à
O
2
tác dụng vừa đủ với 5,82 gam hỗn hợp gồm Mg và kim loại M, thu được 11,36 gam chất rắn X. Hòa tan hết X trong dung dịch HCl (đun nóng, dùng dư 25% so với lượng phản ứng), thu được dung dịch Y. Cho dung dịch NaOH dư vào Y, thấy có 17,60 gam NaOH phản ứng. Biết các phản ứng xảy ra hoàn toàn, hiđroxit của M ít tan trong nước. Cho bi...
Đọc tiếp
Cho 2,24 lít (đktc) hỗn hợp gồm C l 2 v à O 2 tác dụng vừa đủ với 5,82 gam hỗn hợp gồm Mg và kim loại M, thu được 11,36 gam chất rắn X. Hòa tan hết X trong dung dịch HCl (đun nóng, dùng dư 25% so với lượng phản ứng), thu được dung dịch Y. Cho dung dịch NaOH dư vào Y, thấy có 17,60 gam NaOH phản ứng. Biết các phản ứng xảy ra hoàn toàn, hiđroxit của M ít tan trong nước. Cho biết M là kim loại nào sau đây
A. Cu
B. Cr
C. Al
D. Zn